La enfermedad manifiesta tres fases:
- Fase 1: Fase de Respuesta Viral
Esta etapa puede ser asintomática. En caso de presentarse, los síntomas más relevantes son: fiebre, tos, dolor de cabeza, dolor de garganta y diarrea.
Para el 80 % de personas contagiadas con el SARS-CoV-2, esta puede ser la única fase de la enfermedad que se manifieste.
La característica principal de esta etapa es la presencia del virus.
- Fase 2: Fase Pulmonar o Inflamatoria.
En esta fase, los síntomas más relevantes son: respiración entrecortada y síntomas de hipoxia. Ya aparecen imágenes pulmonares anormales.
Cerca del 20 % de los infectados con coronavirus llegan hasta esta etapa.
Una respuesta exacerbada del sistema inmunológico ante la presencia del virus genera una gran inflamación y complicaciones como neumonía. En esta etapa, la mayoría de las personas requieren hospitalización, con un cuadro de neumonía moderada o severa.
Una característica de este período es la baja presencia de virus. En esta instancia de crisis, se recomienda comenzar con el tratamiento de rescate Luarprofeno® para evitar la progresión de la enfermedad.
- Fase 3: Fase de Hiperinflamación.
Se caracteriza por fallas cardíacas y shock con síndrome de distrés respiratorio (ARDS) y presencia de una respuesta inflamatoria sistémica (SIRS).
El 6 % de los casos llegan a esta etapa y presentan un verdadero riesgo de muerte. Cuando la respuesta del sistema inmunológico no puede ser controlada, daña varios órganos del cuerpo. En esta fase, el cuerpo del infectado puede llegar a un shock séptico, en el que los pulmones, los riñones o el hígado sucumben en una falla multiorgánica y coagulación intravascular. En esta etapa se presenta la mortalidad más elevada. Un detalle importante es la ausencia de virus detectable.


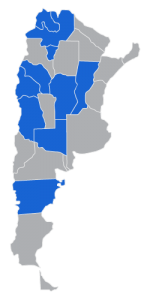 En el marco de la emergencia sanitaria, los Ministerios de Salud de la provincias de Córdoba, Jujuy, La Rioja, Salta, Santa Fe, Tucumán, Mendoza, San Juan, La Pampa y Chubut han autorizado el uso de Luarprofeno ® como tratamiento de rescate bajo uso compasivo.
En el marco de la emergencia sanitaria, los Ministerios de Salud de la provincias de Córdoba, Jujuy, La Rioja, Salta, Santa Fe, Tucumán, Mendoza, San Juan, La Pampa y Chubut han autorizado el uso de Luarprofeno ® como tratamiento de rescate bajo uso compasivo.
